Fino adesso abbiamo trattato il calore come una grandezza legata solamente a fenomeni di scambio termico, collegato alla grandezza temperatura.
In effetti nel passato esso era considerato come una grandezza fisica a se stante che si trasferiva da un corpo all’altro.
In realtà il calore è una forma di energia e Joule, mediante un famoso esperimento, determinò l’equivalenza tra la caloria (la caloria è l’unità di calore che serve per fare innalzare la temperatura di un litro di acqua distillata da 14,5°C a 15,5 °C) e il lavoro meccanico trovando la seguente equivalenza:
1 Cal = 4,186 J
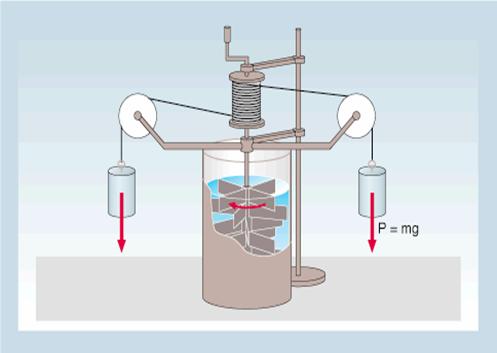
L’apparecchio che utilizzò (Mulinello di Joule) è raffigurato nella seguente figura:
Con tale apparecchiatura è stato possibile determinare l’equivalenza tra l’energia meccanica in gioco legata ai pesi che scendendo di quota percorrono un certo tratto, e l’energia termica legata al moto di agitazione dell’acqua prodotto dalle palette a contatto con essa e messe a loro volta in moto dei pesi.